Задание 9. Взаимосвязь неорганических веществ. ЕГЭ 2026 по химии
Средний процент выполнения: 63.2%
Ответом к заданию 9 по химии может быть последовательность цифр, чисел или слов. Порядок записи имеет значение.
Подпишись на суперполезные материалы

Задачи для практики
Задача 1
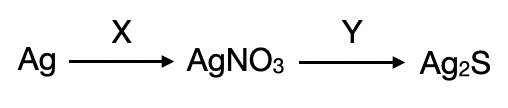
В заданной схеме превращений веществами X и Y являются:
- Fe(NO3)3
- LiNO3
- S
- H2S
- H2SO4
Запишите номера выбранных веществ.
Решение
X: С помощью нитрата железа(III) можно окислить серебро в соль серебра. Это реакция "травления"
Y: Сульфид серебра можно получить обменной реакцией с сероводородом, поскольку образуется устойчивый осадок сульфида серебра
Задача 2
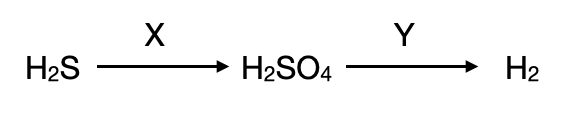
В заданной схеме превращений веществами X и Y являются:
- HNO3
- ZnSO4
- Cu
- Zn
- S
Запишите номера выбранных веществ.
Решение
X: Сероводород окисляется в серную кислоту под действием сильных окислителей, к примеру, азотной кислоты
Y: Водород выделяется при взаимодействии серной кислоты с металлом, стоящим в ряду активности левее водорода
Задача 3
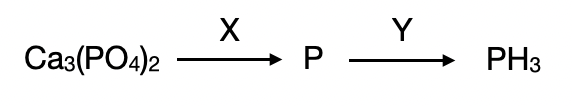
В заданной схеме превращений веществами X и Y являются:
- C
- H2
- KOH
- HNO3
- SiO2
Запишите номера выбранных веществ.
Решение
X: Фосфор из фосфата можно восстановить с помощью сильного восстановителя - углерода
Y: Фосфор не реагирует напрямую с водородом, но растворяется в щелочах с образованием фосфина и гипофосфита
Задача 4

В заданной схеме превращений веществами X и Y являются:
- AgOH
- H2O
- Fe(NO3)2
- Ag2O
- HNO3
Запишите номера выбранных веществ.
Решение
X: Азотная кислота растворяет серебро с образованием нитрата серебра.
Y: При взаимодействии растворимых солей серебра с щелочью образуется оксид серебра(I) и вода, поскольку AgOH неустойчив и распадается при получении
Задача 5
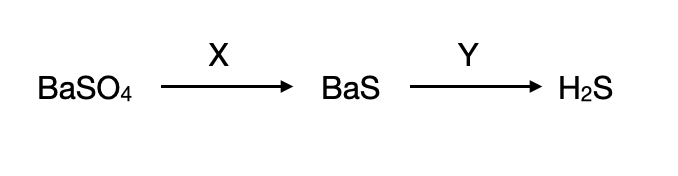
В заданной схеме превращений веществами X и Y являются:
- HNO3
- HCl
- P2O5
- C
- H2
Запишите номера выбранных веществ.
Решение
X: Сульфаты можно восстановить в сульфиды сильными восстановителями, к примеру, углеродом
Y: Сероводород из сульфида бария можно получить обменной реакцией с сильной неокисляющей кислотой, к примеру, соляной
Задача 6
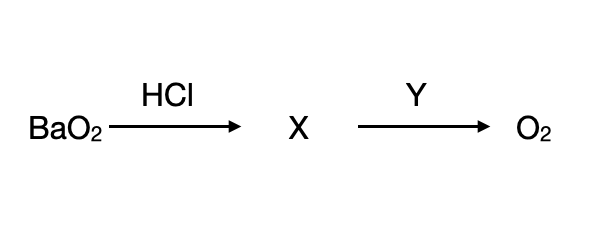
В заданной схеме превращений веществами X и Y являются:
- H2O2
- H2O
- Cl2
- HBr
- H2
Запишите номера выбранных веществ.
Решение
X: Пероксиды металлов при взаимодействии с кислотами образуют перекись водорода
Y: Перекись водорода окисляется в кислород под действием сильных окислителей, например, хлора
Задача 7
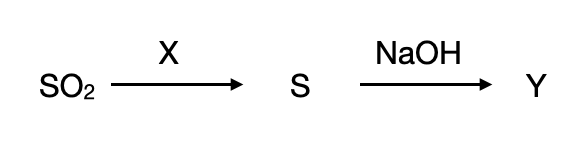
В заданной схеме превращений веществами X и Y являются:
- H2S
- Cl2
- Na2SO4
- Na2SO3
- NaHS
Запишите номера выбранных веществ.
Решение
X: Сера конпропорционирует при взаимодействии сернистого газа и сероводорода в серу
Y: Сера растворяется в щелочах с образованием сульфида и сульфита
Задача 8
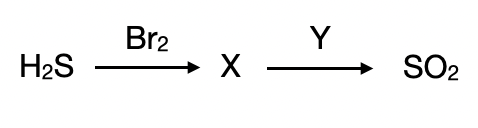
В заданной схеме превращений веществами X и Y являются:
- S
- SO2
- H2SO4(разб)
- O2(изб)
- O2(kat)
Запишите номера выбранных веществ.
Решение
X: Бром окисляет сульфид в серу
Y: Сера в реакции с кислородом без катализатора может образовать только сернистый газ (с катализатором окисление идет до +6)
Задача 9
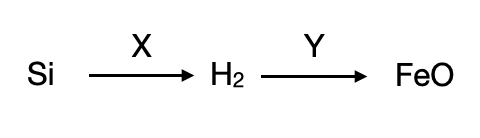
В заданной схеме превращений веществами X и Y являются:
- HNO3
- H2O
- NaOH
- Fe(NO3)3
- Fe3O4
Запишите номера выбранных веществ.
Решение
X: Кремний реагирует с щелочами с образованием растворимых силикатов и водорода
Y: Водород восстанавливает железо(III) из смешанного оксида в оксид железа(II)
Задача 10
Задана следующая схема превращений веществ:
$NaOH →↖{X} Na_2CO_3 →↖{Y} NaCl$
Определите, какие из указанных веществ являются веществами X и Y.
- CaCO3
- HCl
- CO
- CO2
- KCl
Запишите номера выбранных веществ под соответствующими буквами.
Решение
При взаимодействии щелочи и кислотного оксида образуется соответствующая соль, Х - 4.
Для образования хлорида натрия из карбоната нужно провести реакцию ионного обмена, подходит кислота, так как будет выделение углекислого газа. Y - 2.
Задача 11
Задана следующая схема превращений веществ:
$ZnO → X → Y → Zn(OH)_2$
Определите, какие из указанных веществ являются веществами X и Y.
- ZnH2
- ZnSO4
- Zn
- Zn3(PO4)2
- Zn(OH)2
Запишите номера выбранных веществ под соответствующими буквами.
Решение
Из оксида цинка можно получить его металл, используя восстановление водородом или угарным газом. Вещество Х — цинк.
Во второй реакции необходимо получить растворимую соль цинка, например, сульфат цинка. Затем эта соль вступает в РИО со щелочами для образования нерастворимого гидроксида цинка. Вещество Y — cульфат цинка.
Задача 12
Задана следующая схема превращений веществ:
$Al →↖{X} AlCl_3 →↖{Y} Al(OH)_3$
Определите, какие из указанных веществ являются веществами X и Y.
- KOH
- NaCl
- CaCl2
- H2O
- Cl2
Запишите номера выбранных веществ под соответствующими буквами.
Решение
Алюминий надо перевести в хлорид - это можно сделать с помощью хлора (5), соляной кислоты или хлорида менее активного металла. А дальше обменная реакция с образованием нерастворимого гидроксида алюминия. Это делают с помощью растворимых оснований (1)
Задача 13
Задана следующая схема превращений веществ:
$Fe(NO_3)_3 →↖{t°} X →↖{CO_{(изб.)}} Y$
Определите, какие из указанных веществ являются веществами X и Y.
- Fe3O4
- Fe4C3
- Fe2O3
- FeO
- FeCO3
Запишите номера выбранных веществ под соответствующими буквами.
Решение
Разложение нитрата железа(III), поскольку железо среднеактивный металл, идет до оксида железа(III), $NO_2$ и $O_2$. Из оксида железа(III) железо восстанавливается угарным газом - либо до $FeO$ (неполное восстановление), либо до $Fe$ (полное восстановление)
Задача 14
Задана следующая схема превращений веществ:
$FeCl_3 → X → Y → Fe(OH)_3$
Определите, какие из указанных веществ являются веществами X и Y.
- Fe2(SO4)3
- FePO4
- Fe(NO3)3
- Fe2O3
- Fe(OH)2
Запишите номера выбранных веществ под соответствующими буквами.
Решение
При взаимодействии безводного $FeCl_3$ с концентрированной $H_2SO_4$ образуется $Fe_2(SO_4)_3$ и газообразный HCl: $2FeCl_3 + 3H_2SO_{4(конц.} = Fe_2(SO_4)_3 + 6HCl$
Затем сульфат переводим в нитрат: $ Fe_2(SO_4)_3 + 6AgNO_3 = 2Fe(NO_3)_3 + 3Ag_2SO_4$
Затем из нитрата получаем гидроксид: $Fe(NO_3)_3 + 3NaOH = Fe(OH)_3 + 3NaNO_3$
Задача 15
Задана следующая схема превращений веществ:
$FeO →↖{H_2} X →↖{Cl_2} Y$
Определите, какие из указанных веществ являются веществами X и Y.
- FeCl3
- Fe(OH)2
- Fe
- FeCl2
- FeOHCl2
Запишите номера выбранных веществ под соответствующими буквами.
Решение
Железо - среднеактивный металл, поэтому восстанавливается водородом до простого вещества железа. Далее хлор, как сильный окислитель, переводит железо сразу в степень окисления +3.
Задача 16
Задана следующая схема превращений веществ:
$KOH + X → KClO + Y + H_2O$
Определите, какие из указанных веществ являются веществами X и Y.
- HCl
- KClO3
- Cl2
- Cl2O3
- KCl
Запишите номера выбранных веществ под соответствующими буквами.
Решение
В холодной щелочи хлор диспропорционирует близко к себе, потому что как не захотеть в ХОЛОДНОЙ щелочи держать своих поближе, образуются хлорид (степень окисления -1) и гипохлорит (степень окисления +1).
Задача 17
Задана следующая схема превращений веществ:
$ZnCl_2 →↖{NaOH_{(недост.)}} X →↖{t°} Y$
Определите, какие из указанных веществ являются веществами X и Y.
- Zn(OH)2
- Zn
- ZnO
- Na2ZnO2
- ZnH2
Запишите номера выбранных веществ под соответствующими буквами.
Решение
Недостаток щелочи реагирует с солью, содержащей катион, образующий нерастворимый гидроксид, с образованием этого нерастворимого гидроксида. В избытке образуется комплекс, но тут недостаток. Амфотерный гидроксид разлагается на оксид и воду при нагревании.
Задача 18
Задана следующая схема превращений веществ:
$Cu → X →↖{t°} Y → CuSO_4$
Определите, какие из указанных веществ являются веществами X и Y.
- Cu3(PO4)2
- CuO
- Cu(OH)2
- CuH2
- Cu(NO3)2
Запишите номера выбранных веществ под соответствующими буквами.
Решение
Медь переходит в какое-то соединение, которое потом разлагается при нагревании. Растворить медь можно только в окисляющей кислоте. Берем 5, растворив медь в азотке.
Нитрат меди как раз разлагается до оксида меди, который потом можно перевести в сульфат с помощью серной кислоты.
Задача 19
Задана следующая схема превращений веществ:
$Ca →↖{NaOH_{(р-р)}} X →↖{СO_2} Y$
Определите, какие из указанных веществ являются веществами X и Y.
- CaCO3
- CaO
- CaH2
- Ca(OH)2
- Ca(HCO2)2
Запишите номера выбранных веществ под соответствующими буквами.
Решение
Кальций не реагирует с раствором щелочи, но может реагировать с водой с образованием гидроксида кальция, Х - 4.
При взаимодействии основного гидроксида с кислотным оксидом будет образование соли, Y - 1.
Задача 20
Задана следующая схема превращений веществ:
$Fe_2O_3 →↖{X} Fe →↖{Y} FeSO_4$
Определите, какие из указанных веществ являются веществами X и Y.
- H2SO4 (разб.)
- Cu
- H2
- H2SO4 (конц.)
- HI
Запишите номера выбранных веществ под соответствующими буквами.
Решение
Железо восстанавливается в простое вещество железо с помощью водорода. Дальше переход железа в степень окисления +2 можно осуществить вытеснением менее активного металла из сульфата или реакцией с разбавленной серной кислотой (она не окисляющая).
Рекомендуемые курсы подготовки

- 👉 Узнаешь самые алгоритмичные задания в КИМе и научишься их решать.
- 👉 Познакомишься со всеми разделами ЕГЭ и изучишь их основы.
- 👉 Научишься проводить настоящие химические эксперименты.
- 👉 Поймешь, какие формулы нужны на ЕГЭ по химии и как ими пользоваться.
У тебя будет:
- 🤑 Возможность выиграть бесплатный доступ к сентябрьскому курсу.
- ✍️ Домашка после каждого веба без дедлайна (делай, когда тебе удобно).
- 📖 Скрипты, конспекты, множество полезных материалов и лайфхаков.
- 🚀 Удобный личный кабинет: расписание вебов, домашки, твой прогресс и многое другое.
- 😌 Уютная атмосфера, в которой тебе рады!
- 🗣️ Отдельная беседа в ТГ с сокурсниками и преподавателями.
на бесплатном курсе Турбо ЕГЭ







