Задание 21. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная. ЕГЭ 2026 по химии
Средний процент выполнения: 72.8%
Ответом к заданию 21 по химии может быть последовательность цифр, чисел или слов. Порядок записи имеет значение.
Подпишись на суперполезные материалы

Задачи для практики
Задача 1
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
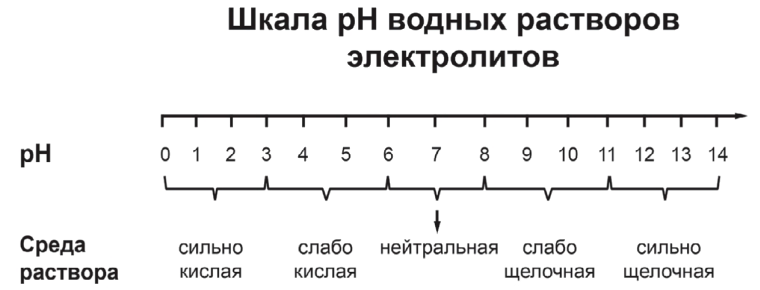
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $LiCl$
2) $RbOH$
3) $KOH$
4) $Na_2SO_3$
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
Решение
Определим характер среды в каждом из растворов:
1) Соль сильной кислоты и сильного основания, среда нейтральная
2) Сильное основание, щелочь, среда сильнощелочная
3) Сильное основание, щелочь, среда сильно щелочная
4) Соль сильного основания и слабой кислоты, среда слабощелочная
У нас получилась некая зависимость, но как выбрать в растворе какой щелочи среда более щелочная? Основность гидроксидов металлов увеличивается сверху вниз по группе, значит среда будет более щелочной в растворе RbOH, а не KOH
Получается, pH растворов веществ увеличивается в порядке 1 - 4 - 3 - 2
Задача 2
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $KHS$
2) $KHSO_4$
3) $BaBr_2$
4) $H_2S$
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
Решение
1) KHS соль образована сильным основанием и слабой кислотой, гидролиз по аниону, среда слабощелочная
2) KHSO4 – соль образована сильным основанием и сильной кислотой, кислая соль сильной кислоты дает на сильнокислую среду
3) BaBr2 – соль образована сильным основанием и сильной кислотой – среда нейтральная
4) H2S – слабая кислота
Задача 3
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $Fe_2(SO_4)_3$
2) $Na_2Cr_2O_7$
3) $LiOH$
4) $HNO_3$
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
Решение
1. $Fe_2(SO_4)_3$ - соль сильной кислоты и слабого основания. Будет идти гидролиз по катиону. Среда слабокислая.
2. $Na_2Cr_2O_7$ - соль сильной кислоты и сильного основания. Гидролиз не протекает. Среда нейтральная.
3. $LiOH$ - щелочь, сильное основание. Среда щелочная.
4. $HNO_3$ - сильная кислота. Среда кислая.
pH уменьшается от щелочной среды к кислой: 3214
Задача 4
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $(NH_4)_2SO_4$
2) $KOH$
3) $KNO_3$
4) $HClO_3$
Запишите номера веществ в порядке увеличения значения pH их водных растворов.
Решение
1) Сульфат аммония. Соль сильной кислоты и слабого основания. Гидролиз по катиону. Среда слабокислая.
2) Гидроксид калия. Сильное основание. Среда щелочная.
3) Нитрат калия. Соль сильного основания и сильной кислоты. Среда нейтральная.
4) Хлористая кислота. Сильная. Среда кислая.
Выстраиваем в ряд по увеличению значения pH: 4, 1, 3, 2
Задача 5
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $LiOH$
2) $SO_2$
3) $KOH$
4) $K_2SO_4$
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
Решение
1) Гидроксид лития. Щелочь. Среда щелочная.
2) Оксид серы(IV). При растворении в воде образует слабую сернистую кислоту. Среда слабокислая.
3) Гидроксид калия. Щелочь. Среда щелочная. Среда будет щелочнее, чем в случае LiOH, поскольку калий находится в группе ниже, чем литий. А значит, основные свойства гидроксида выше.
4) Сульфат бария. Соль сильной кислоты и сильного основания. Гидролиза нет. Среда нейтральная.
Выстраиваем в ряд по уменьшению значения pH: 3, 1, 4, 2
Задача 6
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $NaHCO_3$
2) $CrCl_3$
3) $H_2SO_4$
4) $Cr_2S_3$
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
Решение
NaHCO3 – соль образована сольным основанием (NaOH) и слабой угольной кислотой – среда слабощелочная
CrCl3 – соль образована слабым нерастворимым основанием Cr(ОН)3 и сильной соляной кислотой – среда слабокислая
H2SO4 – сильная кислота, среда сильнокислая
Cr2S3 - соль образована слабым нерастворимым основанием Cr(ОН)3 и слабой сероводородной кислотой – среда нейтральная
Задача 7
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $NH_3$
2) $(NH_4)_2CO_3$
3) $SO_2$
4) $KOH$
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
Решение
Разберем каждое вещество:
1. Аммиак в водном растворе образует гидроксид аммония, слабое основание, pH будет слабощелочной (немного выше 7)
2. Карбонат аммония, соль, гидролизуется и по аниону, и по катиону, pH приблизительно равен 7
3. Сернистый газ в растворе образует слабую сернистую кислоту, pH будет слабокислой (немного ниже 7)
4. Щелочь дает сильнощелочную среду раствора, pH сильно выше 7
Задача 8
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $Ba(OH)_2$
2) $NH_4F$
3) $NH_3$
4) $NH_4NO_3$
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
Решение
Задача 9
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $HClO_3$
2) $FeBr_3$
3) $KOH$
4) $(CH_3COO)_2Ba$
Запишите номера веществ в порядке увеличения значения pH их водных растворов.
Решение
1) Хлорноватая кислота. Сильная. Среда кислая.
2) Бромид железа(III). Соль сильной кислоты и слабого основания. Гидролиз по катиону. Среда слабокислая.
3) Гидроксид калия. Сильное основание. Среда щелочная.
4) Ацетат бария, соль слабой кислоты и сильного основания. Гидролиз по аниону. Среда слабощелочная.
Выстраиваем в ряд по увеличению значения pH: 1, 2, 4, 3
Задача 10
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $H_2Cr_2O_7$
2) $H_2CO_3$
3) $NH_4NO_3$
4) $AgF$
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
Решение
1) Дихромовая кислота. Сильная кислота. Среда кислая.
2) Угольная кислота. Слабая. Среда менее кислая.
3) Нитрат аммония. Соль сильной кислоты и слабого основания. Гидролиз по катиону. Среда слабокислая.
4) Фторид серебра. Соль слабой кислоты и сильного основания. Гидролиз по аниону. Среда слабощелочная.
Выстраиваем в ряд по уменьшению значения pH: 4, 3, 2, 1
Задача 11
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $ZnCl_2$
2) $NaOH$
3) $H_3PO_4$
4) $HNO_3$
Запишите номера веществ в порядке увеличения значения pH их водных растворов.
Решение
1) Хлорид цинка. Соль сильной кислоты и слабого основания. Гидролиз по катиону. Среда слабокислая.
2) Гидроксид натрия. Сильное основание. Среда щелочная.
3) Фосфорная кислота. Слабая кислота. Среда кислая.
4) Азотная кислота. Сильная кислота. Среда еще более кислая.
Выстраиваем в ряд по увеличению значения pH: 4, 3, 1, 2
Задача 12
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $HNO_3$
2) $H_3PO_4$
3) $RbF$
4) $Ba(NO_3)_2$
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
Решение
1) Азотная кислота. Сильная кислота. Среда кислая.
2) Фосфорная кислота. Слабая. Среда менее кислая.
3) Фторид рубидия. Соль слабой кислоты и сильного основания. Гидролиз по аниону. Среда слабощелочная.
4) Нитрат бария. Соль сильной кислоты и сильного основания. Гидролиза нет. Среда нейтральная.
Выстраиваем в ряд по уменьшению значения pH: 3, 4, 2, 1
Задача 13
Для веществ, приведённых в перечне, определите среду их водных растворов с одинаковой молярной концентрацией.
- KF
- $H_2SO_4$
- $Ba(OH)_2$
- $MnSO_4$
Запишите номера веществ в порядке убывания значения pH их водных растворов.
Решение
- Соль, образованная сильным основанием и слабой кислотой. Среда слабощелочная.
- Сильная кислота. Среда сильнокислая.
- Сильное основание - сильнощелочная среда.
- Соль, образованная слабым основанием и сильной кислотой. Среда слабокислая.
Задача 14
Для веществ, приведённых в перечне, определите среду их водных растворов с одинаковой молярной концентрацией.
- нитрат бария
- хлорид железа(III)
- хлорид водорода
- ацетат калия
Запишите номера веществ в порядке убывания значения pH их водных растворов.
Решение
Вещества 1,2 и 4 являются солями, а вещество 3 - сильная соляная кислота. У кислоты будет самый низкий pH. В случае остальных солей смотрим на гидролиз:
Нитрат бария не гидролизуется, pH нейтральный.
Хлорид железа(III) гидролизуется по катиону, pH слабокислый.
Ацетат калия гидролизуется по аниону, pH слабощелочной
Итоговая последовательность по уменьшению pH: 4123
Задача 15
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите среду их водных растворов с одинаковой молярной концентрацией.
- Cu(NO3)2
- Li2S
- NaOH
- CaCl2
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
Решение
- Соль, образованная слабым основанием и сильной кислотой. Среда слабокислая.
- Соль, образованная сильным основанием и слабой кислотой. Среда слабощелочная.
- Сильное основание - сильнощелочная среда.
- Соль, образованная сильным основанием и сильной кислотой. Среда нейтральная.
Задача 16
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите среду их водных растворов с одинаковой молярной концентрацией.
- FeCl3
- Ca(OH)2
- KF
- BaCl2
Запишите номера веществ в порядке убывания значения pH их водных растворов.
Решение
Задача 17
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $H_2SO_4$
2) $KMnO_4$
3) $NH_4OH$
4) $Ba(NO_2)_2$
Запишите номера веществ в порядке увеличения значения pH их водных растворов.
Решение
Разберемся какую среду раствора создают эти вещества:
А) Сильная кислота, среда сильнокислая
Б) Соль сильного основания и сильной кислоты, гидролиза нет, среда нейтральная
В) Слабое растворимое основнание, среда щелочная
Г) Соль сильного основания и слабой кислоты, среда слабощелочная
Задача 18
Установите соответствие между исходными веществами, условиями электролиза и продуктами электролиза: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
| ВЕЩЕСТВА И УСЛОВИЯ ЭЛЕКТРОЛИЗА | ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
| А) раствор хлорида кальция с графитовыми электродами Б) раствор сульфата меди(II) с графитовыми электродами В) раствор сульфата меди(II) с медными электродами Г) раствор сульфата цинка c цинковыми электродами |
1) Cl2, H2 2) Сa(OH)2, Cl2, H2 3) Cu, O2, H2SO4 4) Cu, H2, O2, H2SO4 5) анод растворяется, на катоде выделяется металл 6) анод растворяется, на катоде выделяются металл и водород |
Запишите выбранные цифры под соответствующими буквами.
Решение
В случае раствора хлорида на аноде выделится хлор. Из растворов сульфатов на аноде выделится кислород. Металлические аноды будут при этом растворяться. На катоде в случае кальция будет выделяться водород (т.к. Ca - активный металл), в случае меди будет выделяться сама медь (т.к. Cu - малоактивный металл), в случае цинка - будет происходить одновременное образование металла и водорода.
Задача 19
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $Li_2S$
2) $KClO_3$
3) $HBrO_4$
4) $NaOH$
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
Решение
1) Сульфид лития, соль слабой кислоты и сильного основания. Гидролиз по аниону. Среда слабощелочная.
2) Хлорат калия, соль сильной кислоты и сильного основания. Гидролиза нет. Среда нейтральная.
3) Бромная кислота. Сильная. Среда кислая.
4) Щелочь - среда щелочная.
Выстраиваем в ряд по уменьшению значения pH: 4, 1, 2, 3
Задача 20
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.

Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) $SO_2$
2) $BaO$
3) $NH_3$
4) $SO_3$
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
Решение
Определим характер среды в каждом из растворов:
1) Сернистый газ при растворении в воде образует сернистую кислоту. Она слабая
2) Оксид бария при растворении в воде образует сильное основание гидроксид бария.
3) Аммиак при растворении в воде образует слабое основание гидроксид аммония
4) Серный газ при растворении в воде образует сильную серную кислоту.
Рекомендуемые курсы подготовки

- 👉 Узнаешь самые алгоритмичные задания в КИМе и научишься их решать.
- 👉 Познакомишься со всеми разделами ЕГЭ и изучишь их основы.
- 👉 Научишься проводить настоящие химические эксперименты.
- 👉 Поймешь, какие формулы нужны на ЕГЭ по химии и как ими пользоваться.
У тебя будет:
- 🤑 Возможность выиграть бесплатный доступ к сентябрьскому курсу.
- ✍️ Домашка после каждого веба без дедлайна (делай, когда тебе удобно).
- 📖 Скрипты, конспекты, множество полезных материалов и лайфхаков.
- 🚀 Удобный личный кабинет: расписание вебов, домашки, твой прогресс и многое другое.
- 😌 Уютная атмосфера, в которой тебе рады!
- 🗣️ Отдельная беседа в ТГ с сокурсниками и преподавателями.
на бесплатном курсе Турбо ЕГЭ







